光谱学基础-历史、解释和应用
原子光谱学涉及原子与光的相互作用;
而分子光谱学涉及分子与光的相互作用。
原子光谱学提供有关样品的原子或元素身份的信息;
而分子光谱学可以揭示有关分子身份和分子结构的信息。
涉及原子光谱与分子光谱的跃迁类型不同:
在原子光谱中,通常观察到的是电子态跃迁;
而在分子光谱中,除了电子态跃迁外,还可以研究振动和旋转跃迁。
本文重点介绍分子光谱。
光谱实验装置
根据所用技术的不同,光谱实验的单位也不同。
图1列出了电磁(EM)光谱中的一些关键区域、这些区域内常用的一些光谱技术、每种技术探测的跃迁类型以及使用的单位。
例如,紫外可见吸收光谱涉及分子中价电子的跃迁,以波长(λ)为单位报告,如纳米(nm)
或埃(A)。
红外吸收光谱则研究分子振动,通常以波数(cm-1)为单位报告。

图1:电磁频谱(EM)、使用的光谱技术、涉及的跃迁和光谱单位。EM图像取自参考文献1
吸收光谱学是电磁辐射因与物质相互作用而随频率变化的吸收过程。
想象一下,样品在比色皿中与不同类型的光相互作用,如图2所示。当样品吸收不同类型光时,会激发出不同类型的跃迁。
例如:
X射线激发的是原子核电子的跃迁,
紫外光激发的是价电子的跃迁,
红外辐射激发的是分子振动,
微波区域激发的是分子旋转,
在射频(RF)下则激发电子和原子核。
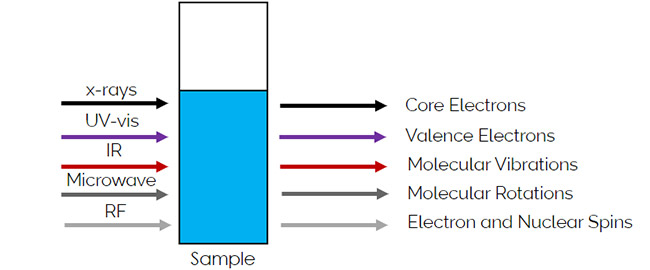
图2:根据所用光的类型,激发分子的不同类型的跃迁。
紫外-可见吸收光谱
紫外-可见吸收光谱在分子中涉及激发分子轨道之间的价电子。
两个重要的分子轨道是最高占据分子轨道(HOMO)和最低未占分子轨道(LUMO)。
对于处于基态的分子,HOMO被电子占据,而LUMO则没有。
在紫外-可见吸收实验中,一个电子会从HOMO激发到LUMO。当从基态激发到激发态时,还可以发生振动和旋转跃迁。
紫外可见吸收光谱仪由宽带光源、色散元件、波长选择器、检测器和记录器组成,如图3.2所示
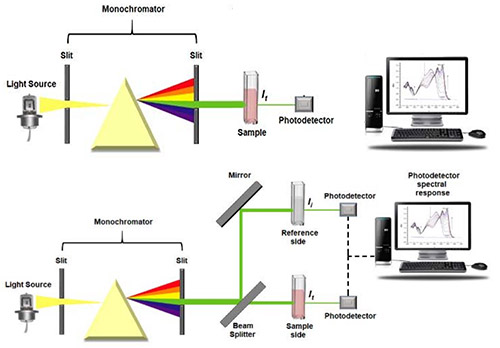
图3:单光束(上)和双光束(下)UV-Vis分光光度计。图摘自参考文献2
在紫外可见光谱实验中,通过计算透过参比样品的光强度与透过样品的光强度之比的对数,来计算样品的吸光度A,其中,透过参比样品的光强度与透过样品的光强度之比是随波长变化的函数:
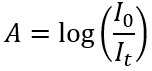
这可用于使用比尔-朗伯定律或比尔定律计算样品中吸收物质的浓度:

其中,ε是摩尔吸光系数,表示样品中吸收物质对特定波长光的吸收强度,通常以M-1cm-1表示。c是吸收物质的浓度,单位为摩尔浓度M,d是光与样品相互作用的距离(有时称为路径长度)。比尔定律在吸光度介于0.2至0.8之间时效果最佳。双光束紫外-可见光谱仪通过使用分束器同时激发参比和样品,使这一测量更加便捷。这使得可以同时收集参比和样品的强度。
比尔定律的一个例子是用于测量样品中的蛋白质浓度,例如在重组蛋白生产中发现的样品。蛋白质含有如苯丙氨酸、色氨酸和酪氨酸等氨基酸,这些氨基酸具有芳香基团,在紫外光下吸收强烈。通过在280纳米处测量样品的吸收并应用比尔定律,可以估算出蛋白质的浓度,如图4.3所示。尽管这种方法可能不够准确,因为核酸材料通常存在于这些样品类型中,且会吸收紫外线,但考虑到不同蛋白质中这些氨基酸的比例不同,该方法仍可用于监测重组蛋白产品的纯化过程。商用的纯化仪器,如HPLC系统,通常使用基于紫外可见光谱的检测。
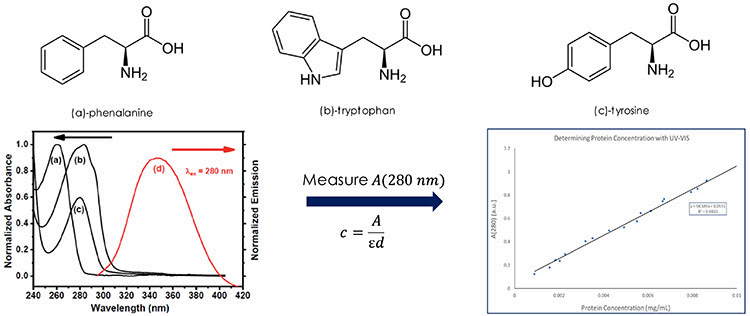
图4:用于通过紫外-可见光谱法测定蛋白质浓度的三种氨基酸。左侧图表显示了(a)苯丙氨酸、(b)色氨酸、(c)酪氨酸的紫外-可见吸收光谱。右侧图表显示了根据比尔定律获得的280纳米处的吸光度与蛋白质浓度的关系。紫外-可见吸收光谱数据来自参考文献3。
光致发光——荧光和磷光
光致发光是指物质吸收光子后发出的光。
它分为两种类型:荧光和磷光。
荧光相对较强且快速,时间尺度在皮秒(ps)到纳秒(ns)之间。
相比之下,磷光较弱且缓慢,时间尺度在微秒(μs)或更长。
与激发波长相比,荧光和磷光都会发生红移。
Jablonski图,以Aleksander Jabłonski命名,是理解分子中不同类型的光物理过程的有用工具,如图54所示。本图描述了分子的基态和激发态电子状态、基态和激发态电子状态内的振动和转动能级、这些状态的电子自旋性质以及所有这些状态之间可能发生的跃迁类型。
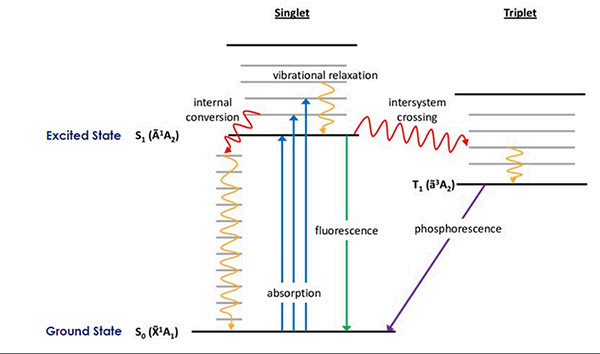
图5:Jablonski图,描述了分子中可能的光物理过程。图片摘自参考文献4。
当一个处于激发态的电子通过发射光子而从激发态回到基态时,就会产生荧光。
当基态和激发态都是单重态时,就会发生荧光。
还可能发生的是,处于单重态的电子在受到电激发后,可以通过系统间跃迁(IC)进入一个电子激发的三重态自旋状态。根据量子力学原理,激发的三重态电子通过直接光子发射弛豫到基态是被禁止的。然而,由于自旋-轨道耦合的作用,这种类型的跃迁确实会发生,这一过程正是磷光的起源。
荧光光谱仪的示意图如图6.5所示。光源可以是宽带光源或窄带激光器,通过透镜聚焦到样
品上,样品中的电子从基态激发到激发态。当电子从激发态弛豫到基态并发射一个光子
时,通过放置一个透镜收集发出的荧光,通常该透镜与激发路径呈90度角,以减少来自激
发源的背景干扰,并将荧光聚焦到单色仪中进行检测。然后数据被发送到记录器,在那里
测量的荧光以发射光强度随发射波长的变化形式报告。
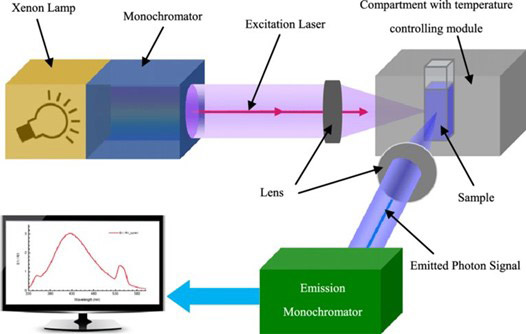
图6:荧光光谱仪示意图。图片摘自参考文献5。
以荧光素的吸光度和荧光光谱为例,如图7.6所示。荧光素是一种用于生物成像的染料。吸收光谱用蓝色表示,荧光光谱用红色表示。可以看出,荧光光谱相对于吸收光谱发生了红移。这被称为斯托克斯位移。荧光光谱还像是吸收光谱的倒置,这是荧光实验中常见的现象。
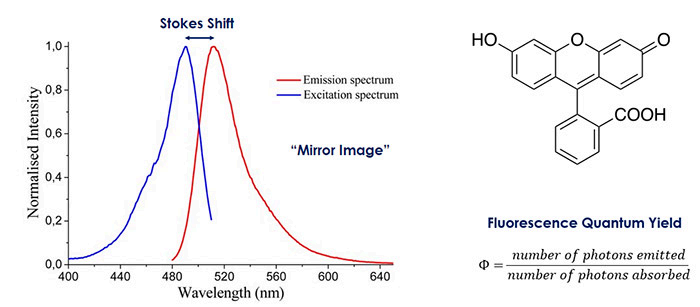
图7:荧光素的吸收(蓝色)和荧光(红色)光谱。荧光光谱从吸收光谱中红移,并且呈现为“镜像”形式。光谱摘自参考文献6。
荧光测量中一个重要量是荧光量子产率Φ,即分子发射的光子数除以分子吸收的光子数:
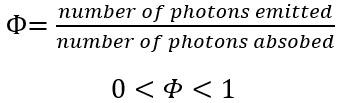
Φ的最大值为1,此时分子每吸收一个光子就发射一个光子;最小值为0,此时分子不发射任何光子。
可以使用脉冲激光和时间分辨检测方案进行时间分辨荧光测量。近红外荧光蛋白( iRFP)是一类用于生物成像的基因工程荧光探针。几种iRFP的稳态吸收和荧光光谱如图8.7所示。
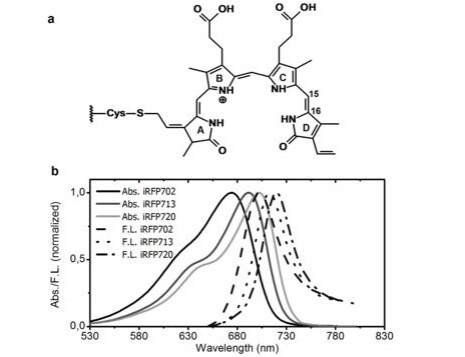
图8:近红外荧光蛋白的左稳态荧光光谱。摘自参考文献7。
这些蛋白质吸收和荧光都偏向NIR方向,因此特别适用于深层组织成像,因为长波长的光比短波长的光能穿透更深的组织。图9.7展示了iRFP702在H2O and D2O中,激发波长为660 nm, 发射波长702 nm的时间分辨荧光光谱。
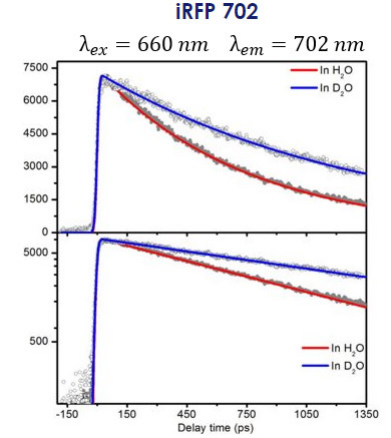
图9:iRFP 702在660 nm处发射并在702 nm处检测到的时间依赖性荧光光谱在水(红色)和D2O中显示了动力学同位素效应。底部的曲线是相同的衰减曲线,但强度采用对数刻度。取自参考文献7。
可见荧光强度随时间衰减,衰减时间从几百皮秒(ps)到几十纳秒(ns)不等,这种时间依赖性荧光强度可描述为:
![]()
其中,I(t)是激发后时间t的荧光强度,Io是初始荧光强度,τ是荧光寿命,即I(t)达到初始值(Io)的1/e的强度所需的时间。
iRFP 702在两种溶剂中的荧光寿命不同。在水溶液中,测得的荧光寿命为749皮秒,而在氘水中则为1.35纳秒。氘水中的荧光寿命比水溶液长,这可以归因于较重的氘同位素的存在,导致这两种溶剂中iRFP 702的荧光寿命的动力学同位素效(KIE)应为1.8。
福斯特Förster共振能量转移(FRET)是两种荧光团之间发生的荧光过程。在FRET中,两个荧光团被放置得非常接近,其中一个荧光团(FRET供体)的发射光谱与另一个荧光团(FRET受体)的吸收光谱重叠,形成一个FRET对。当供体分子从基态激发到激发电子态时,可能会发生非辐射能量转移,供体激发受体,随后受体荧光,如图10.8所示。
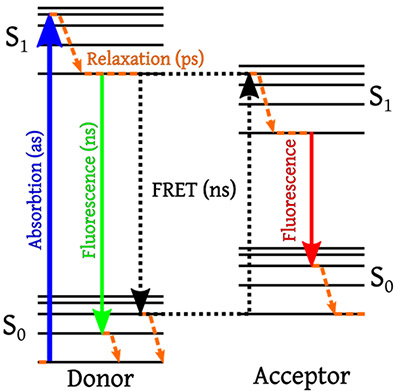
图10:显示FRET对之间Forster共振能量转移的Jablonski图。图片摘自参考文献8。
FRET的效率高度依赖于距离,随1/r^6变化,其中r是供体和受体之间的距离。由于这种强烈的距离依赖性,FRET仅在供体和受体相距几纳米时发生,在超分辨率定位成像以及检测和追踪蛋白质相互作用中具有应用。
磷光被广泛用于表征“下一代”材料,如纳米材料、低密度材料和新型半导体。这些材料在光伏、能源生成和太阳能电池中有着广泛的应用。磷光实验的设置与荧光实验非常相似,如图11所示。
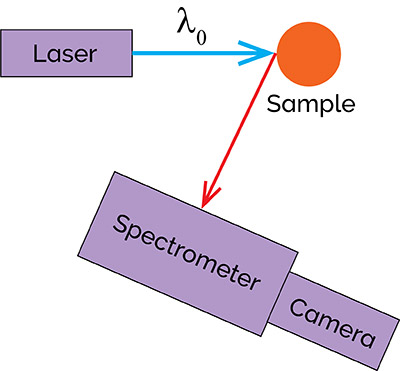
图11:磷光光谱仪示意图。
氮化镓纳米结构是下一代材料的一个例子,因其磷光发射在蓝色范围内而受到关注,这使得它们成为用于蓝色LED和基于二极管的激光器的理想候选材料。如图129所示,磷光被用来表征氮化镓纳米结构的质量。通过使用xy平移台,研究人员能够生成磷光整体强度的地图,并通过监测370 nm处缺陷带的存在或不存在来识别纳米结构中的缺陷,此外还有360 nm处的正常磷光发射。
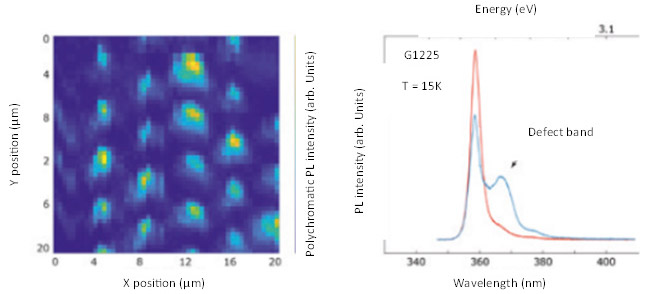
图12:左下角-基于氮化镓的纳米结构阵列的总PL强度随xy位置的变化。右下角-基于氮化镓的纳米
结构阵列的代表性PL光谱,显示主要PL发射波长为~360 nm,检测带宽为~370 nm。改编自参考文献9。
研究人员一直在寻找替代传统晶体硅的材料,用于薄膜太阳能电池板中的薄膜吸收层,以降低生产成本并提高可持续性。铜锌锡硫化物(CZTSSe)被认定为一种可行且特别有吸引力的候选材料,因为它仅由低毒性的丰富材料组成。通过定量磷光可以获取这些材料电子结构的信息,从而预测使用这种材料时设备的开路电压。这一点很重要,因为可以在生产过程早期进行测量,而无需制造整个太阳能电池装置来获得这些信息。
在图13所示的实验中,10到12名研究人员通过引入一层称为缓冲层的半导体材料,能够改变CZTSSe的电子特性,并使用定量磷光技术监测这些变化的影响。利用几种缓冲层对1.05电子伏特以下磷光强度的影响,最终预测了不同缓冲层下材料在器件中的性能。
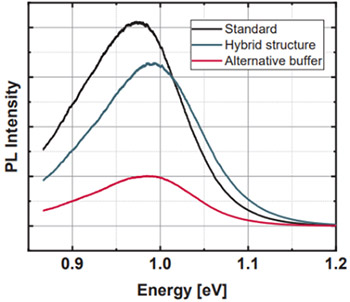
图13:在铜锌锡硫化物(CZTSSe)吸收器上测量的底部-PL光谱,使用了多种缓冲液。改编自参考文献10-12。
拉曼光谱技术
拉曼光谱可以作为分子振动和旋转的高度敏感探针。这一技术最初由印度物理学家C.V.拉曼发现,他在1928年发表于《自然》杂志的一篇题为“辐射的负吸收”的论文中公布了研究成果。
与红外吸收光谱不同,后者通过直接吸收能量等于分子振动和旋转跃迁的红外光 来探测分子的振动和旋转,拉曼光谱的工作原理则有所不同。
在拉曼实验中,使用一个不与分子中的任何振动或旋转状态共振的激发源,将分子中的电子激发到电子虚态,从而产生散射事件。
最常见的散射事件是瑞利散射,即光子与分子弹性散射,且这些光子的能量在散射后不会改变。
然而,光子可以与分子发生非弹性散射,在这种情况下,散射后光子的能量减少相当于分子的一个振动或旋转能级——这被称为斯托克斯拉曼散射。此外,光子也可以与分子发生非弹性散射并获得能量,此时获得的能量相当于分子的一个振动或旋转能级。这被称为反斯托克斯散射。无论是斯托克斯散射还是反斯托克斯散射,效率都相对较低,大约只有10^-7的光子会发生非弹性散射。这些不同的过程如图14.13所示。
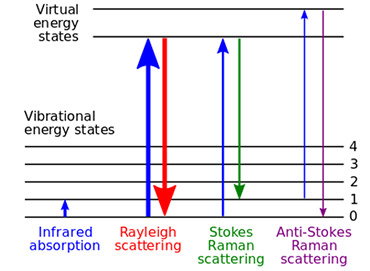
图14:拉曼光谱中的能量水平和散射事件。摘自参考文献13。
图1514显示了拉曼光谱仪的示意图。用光激发样品,产生的散射光通过滤波器降低瑞利散射的强度,然后进入光谱仪,在那里分散并由探测器收集和记录。
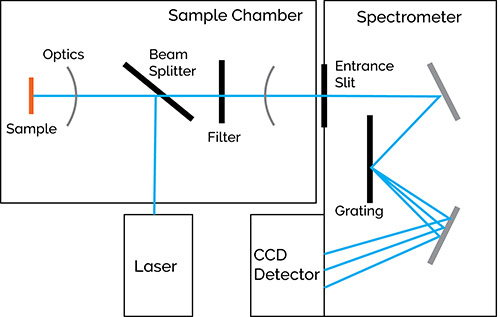
图15:拉曼光谱仪示意图。摘自参考文献14。
拉曼光谱中常用的单位是波数(cm-1)。然而,拉曼光谱的独特之处在于,样品中振动或旋转跃迁对应的单位总是相对于激发源的能量,即瑞利线来报告。例如,假设在435.83纳米激发时观察到一个未知的拉曼带位于457.4纳米。根据公式:
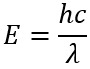
其中h为普朗克常数,c为光速,λ为光波长,激发源的能量为:
![]()
而非弹性散射光的能量为:
![]()
这导致了1082 cm-1的能量,从而产生了在457.4 nm处的未知带:
![]()
拉曼信号基于散射事件,其强度与激发波长的四次方成反比,即1/λ4,因此使用较低波长的激发源可以增加拉曼信号的强度。
拉曼“光谱密度”,即在给定能量下,拉曼模式在波长空间中的相互接近程度,在很大程度上取决于激发源的波长以及所研究模式的光谱区域。
例如,考虑一个实验目标是使用拉曼光谱测量能量范围从0到4000 cm-1的分子振动和旋转。
如果选择262纳米作为激发源,则最高能量模式在4000 cm-1处会出现在292.7纳米,即比激发源红移~30纳米。
然而,如果选择785纳米作为激发源,则同一模式在4000 cm-1处会出现在1144纳米,红移接近360纳米。
这种光谱密度对激发波长的依赖性要求在设计拉曼实验时,应仔细考虑光谱仪的带宽和分辨率以及所用探测器的波长依赖量子效率。
拉曼光谱是一种高度特异性的非破坏性技术,这种特性可以用来以多种方式表征材料。
它可以用来识别未知化学物质,如图16.15所示的六氯苯。
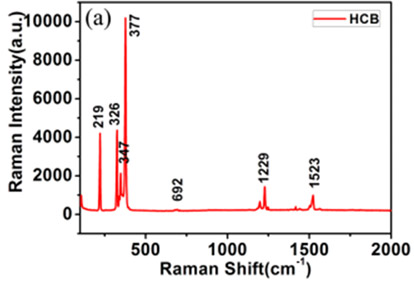
图16:六氯苯的拉曼光谱。摘自参考文献15。
它还可以用作量化过渡金属二硫属化物(TMDC)型单层的化学成分的一种方法,如MoS2和WS2,通过测量Mo1-xWxS2单层合金中Mo相对于W的摩尔分数,如图17.16所示。

图17:Mo1-xWxS2单层合金的拉曼光谱,随W与Mo摩尔分数的变化。摘自参考文献16。
多层纳米材料的增长也可以通过观察MoS2中拉曼模式随层数变化的情况来监测,如图18.17所示。当材料中的层数从1增加到4时,拉曼光谱中会出现额外的模式,这些模式归因于材料中的呼吸和剪切模式。这些模式涉及多层之间的运动以及一层运动对另一层的影响。这种依赖于多层的运动仅在具有多个层次的样品中才可能出现,在单层拉曼光谱中并不存在。
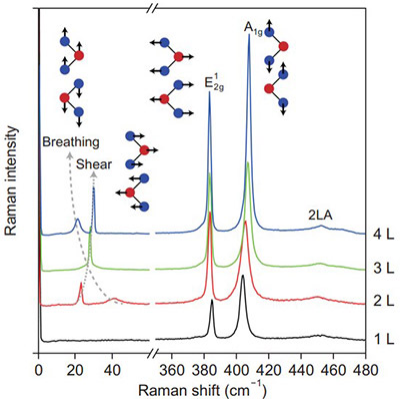
图18:二硫化钼的拉曼光谱随层数的变化。随着层数的增加,更多的拉曼模式变得明显。摘自参考文献17。
分子结构的差异,如水和冰中的差异,也可以通过拉曼光谱来表征。尽管水和冰的化学组成相同,但图19.18显示,水的拉曼光谱中O-H伸缩带比冰宽得多,这反映了水中的OH基团可以自由探索更多的振动和旋转子空间,而在冰中则更为受限。
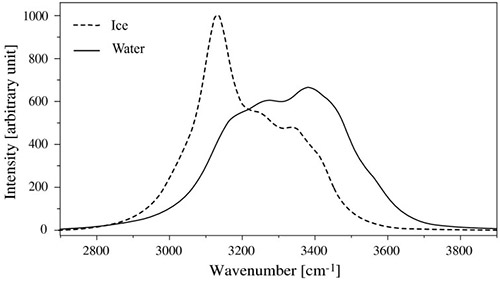
图19:水和冰的拉曼光谱,显示了液相与固相中OH伸缩模式线形的依赖性。摘自参考文献18。
拉曼光谱可用于测量材料中的应变和缺陷。图20比较了纯石墨与经过长时间球磨处理的石墨样品的拉曼光谱。19在石墨中观察到的二维带在24小时球磨后,其双峰轮廓被抑制并转化为单峰,“类似突起”的模式。
拉曼光谱特征的细微差异可用于区分非常相似的材料,如石墨烯和石墨。石墨烯是由原子以六角晶格纳米结构排列而成的一层单分子层,而石墨则由多层石墨烯堆叠而成。图20.20展示了N掺杂石墨烯和高度取向热解石墨(HOPG)的拉曼光谱。N掺杂石墨烯中的二维带相对于石墨的二维带略有红移。此外,石墨中存在多个模式,导致其二维带的线形与石墨烯不同。这种差异是由于石墨中含有多层石墨烯。N掺杂石墨烯中观察到的D带被称为缺陷或无序带,归因于样品中的氮掺杂。

图20:(a):N掺杂石墨烯(上)和高取向热解石墨(HOPG)(下)的拉曼光谱。(b):N掺杂石墨烯和HOPG的二维能带放大图,显示了两种材料线形的差异。摘自参考文献20。
金属和半导体单壁碳纳米管(SWCNT)也可以通过拉曼光谱进行区分。图21顶部的曲线显示了金属SWCNT的拉曼光谱,而底部的曲线则展示了半导体SWCNT的拉曼光谱。21金属样品与半导体样品的G模式光谱展宽程度不同,用于区分两种类型的SWCNTs。
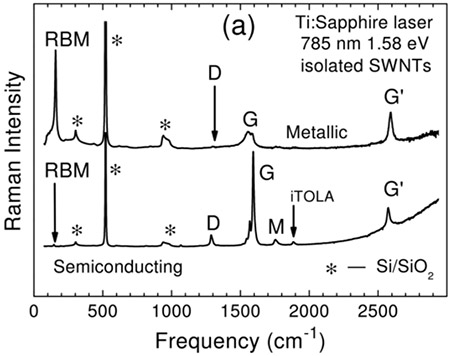
图21:金属(上)和半导体单壁碳纳米管(SWCNT)的拉曼光谱。拉曼光谱中的差异,如G带的展宽,可用于区分金属和半导体类型的样品。摘自参考文献21。
参考文献:
- https://commons.wikimedia.org/wiki/File:EM_Spectrum_Properties_edit.svg
- Sergio Braga, Mauro & Gomes, Osmar & Jaimes, Ruth & Braga, Edmilson & Borysow, Walter & Salcedo, Walter. (2019). Multispectral colorimetric portable system for detecting metal ions in liquid media. 1-6. 10.1109/INSCIT.2019.8868861.
- Mahalingam, Venkataramanan & Hazra, Chanchal & Samanta, Tuhin. (2014). A Resonance Energy Transfer Approach for the Selective Detection of Aromatic Amino Acids. J. Mater. Chem. C. 2. 10.1039/C4TC01954G.
- Ernest, Cheryl. (2011). High-Resolution Studies of the ùA₂– X̃¹A₁Electronic Transition of Formaldehyde: Spectroscopy and Photochemistry.
- Li, Changzheng & Yue, Yanan. (2014). Fluorescence spectroscopy of graphene quantum dots: Temperature effect at different excitation wavelengths. Nanotechnology. 25. 435703. 10.1088/0957-4484/25/43/435703.
- Bennet, Mathieu. (2011). MULTI-PARAMETER QUANTITATIVE MAPPING OF MICROFLUIDIC DEVICES.
- Zhu J, Shcherbakova DM, Hontani Y, Verkhusha VV, Kennis JT. Ultrafast excitedstate dynamics and fluorescence deactivation of near-infrared fluorescent proteins engineered from bacteriophytochromes. Scientific Reports. 2015 Aug;5:12840. DOI: 10.1038/srep12840. PMID: 26246319; PMCID: PMC4526943.
- FRET Jablonski diagram.svg – Wikimedia Commons Creative Commons — Attribution-ShareAlike 3.0 Unported — CC BY-SA 3.0
- J. Malindretos, C. Hilbrunner, A. Rizzi, IV. Physikalisches Institut, Festkörper und Nanostrukturen, Georg-August-Universität Göttingen, Germany (April 2019).
- David Regesch, Levent Gütay, […], and Susanne Siebentritt, Appl. Phys. Lett. 101, 112108 (2012), Degradation and passivation of CuInSe2.
- Levent Gütay, David Regesch, […], and Susanne Siebentritt, Appl. Phys. Lett. 99, 151912 (2011), Influence of copper excess on the absorber quality of CuInSe2.
- Thomas Unold, Levent Gütay, Wiley, Book chapter 11: Photoluminescence Analysis of Thin‐Film Solar Cells, Book: Advanced Characterization Techniques for Thin Film Solar Cells.
- Raman energy levels.svg – Wikimedia Commons Creative Commons — Attribution-ShareAlike 3.0 Unported — CC BY-SA 3.0
- Schmid, Thomas & Dariz, Petra. (2019). Raman Microspectroscopic Imaging of Binder Remnants in Historical Mortars Reveals Processing Conditions. Heritage. 2. 1662-1683. 10.3390/heritage2020102.
- Zhang, Xian & Zhou, Qin & Huang, Yu & Li, Zhengcao & Zhang, Zhengjun. (2011). Contrastive Analysis of the Raman Spectra of Polychlorinated Benzene: Hexachlorobenzene and Benzene. Sensors (Basel, Switzerland). 11. 11510-5. 10.3390/s111211510.
- Chen, Yanfeng & Dumcenco, Dumitru & Zhu, Yiming & Zhang, Xin & Mao, Nannan & Feng, Qingliang & Zhang, Mei & Zhang, Jin & Tan, Ping-Heng & Huang, ying-sheng & Xie, Liming. (2014). Composition-dependent Raman modes of Mo1−xWxS2 monolayer alloys. Nanoscale. 6. 10.1039/c3nr05630a.
- Lee, Changgu & Yan, Hugen & Brus, Louis & Heinz, Tony & Hone, James & Ryu, Sunmin. (2010). Anomalous Lattice Vibrations of Single- and Few-Layer MoS2. ACS nano. 4. 2695-700. 10.1021/nn1003937.
- Claverie, Rémy & Fontana, Marc & Durickovic, Ivana & Bourson, Patrice & Marchetti, Mario & Chassot, Jean-Marie. (2010). Optical Sensor for Characterizing the Phase Transition in Salted Solutions. Sensors (Basel, Switzerland). 10. 3815-23. 10.3390/s100403815.
- Kaniyoor, Adarsh & Sundara, Ramaprabhu. (2012). A Raman spectroscopic investigation of graphite oxide derived graphene. AIP Advances. 2. 032183-032183. 10.1063/1.4756995.
- He, Chunyong & Li, Zesheng & Cai, Maolin & Cai, Mei & Wang, Jian-Qiang & Tian, Zhiqun & Zhang, Xin & Shen, Pei. (2012). A strategy for mass production of selfassembled nitrogen-doped graphene as catalytic materials. J. Mater. Chem. A. 1. 1401-1406. 10.1039/C2TA00807F.
- Dresselhaus, M.S., Dresselhaus, A.G., & Jorio, A. (2007). Raman Spectroscopy of Carbon Nanotubes in 1997 and 2007. Journal of Physical Chemistry C, 111, 17887-17893.
- Tambraparni, Bindu & Wang, Shiren. (2010). Separation of Metallic and Semiconducting Carbon Nanotubes. Recent patents on nanotechnology. 4. 1-9. 10.2174/187221010790712084.
原文链接:
https://andor.oxinst.com/learning/view/article/fundamentals-of-spectroscopy-history-explanations-and-applications
